在雷竞技raybat竞猜西安市计算生物信息学重点实验室里,高琳教授团队青年教师李朋勇正带领学生们沉浸在人工智能辅助药物研发的前沿研究中。近日,他们的研究成果以“一种通过反应性分子砌块进行合理配体生成与毒性控制的深度学习方法(A deep learning approach for rational ligand generation with toxicity control via reactive building blocks)”为题,登上了国际TOP期刊 Nature Computational Science,为药物设计领域带来了革新。

西电雷竞技raybat竞猜西安市计算生物信息学重点实验室合照,左6为高琳教授,右1为李朋勇副教授
由DEL技术引发的灵感
近年来,人工智能技术,特别是深度学习模型,已在药物设计领域引起了广泛关注。然而,由于化学空间的复杂性,现有方法难以精确捕捉合理的药物分子模式,导致生成的药物常面临合成难度大、毒性高等问题。如何设计出合理的药物分子,并让其性质可控,仍是当前亟待解决的挑战。
DNA编码化合物文库(DEL)技术是一项在药物发现领域已经相当成熟的湿实验技术。它通过将DNA片段与化合物结合,形成一个庞大的化合物库,每个化合物都携带着独特的DNA“条形码”,可以快速筛选出与靶标蛋白结合的分子。
“DEL技术的高效筛选能力启发了我,”李朋勇回忆道,“但同时,我也意识到它的一些局限性,比如化合物库的规模有限。”
这激发了李朋勇的思考,他开始考虑如何克服现有深度学习模型和DEL技术的不足。“我一直在想,有没有一种方法,可以既保留DEL的高效性,又能够精确控制药物分子的性质?”李朋勇说。
DeepBlock方法的诞生
经过无数次的思考和实验,李朋勇和他的团队最终提出了DeepBlock方法。这一方法的核心在于参照DEL,利用分子砌块(Reactive Building Blocks)的可反应性来生成可合成的配体分子。
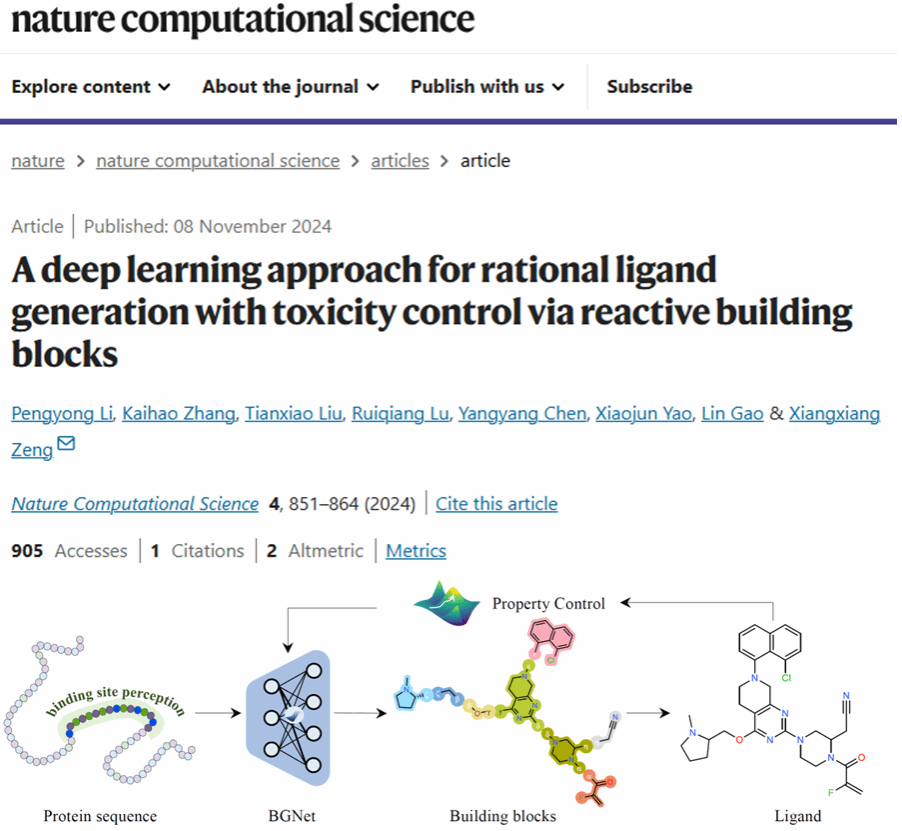
DeepBlock方法的示意图,展示了分子砌块如何通过深度学习算法拼接成目标配体分子
分子砌块,顾名思义,就是构成药物分子的基本“建筑模块”。这些模块通常是一些具有特定化学性质的简单分子或分子片段,它们可以通过化学反应相互连接,形成更复杂的分子结构。
“分子砌块就像是乐高积木,我们可以根据目标蛋白质序列,将这些‘积木’拼接成具有特定药理活性的药物分子。”李朋勇解释道,“通过这种方式,我们不仅能保证生成的分子的可合成性,还能通过靶点感知的分子优化方法,控制分子的毒性。”
DeepBlock方法的实现并非一蹴而就。团队成员们首先需要构建一个庞大的分子砌块数据库,并设计出一种有效的算法来模拟分子拼接过程,然后利用深度学习模型,从海量的化合物数据中学习药物分子模式,去生成理想的配体分子。
“我们在模型训练和参数调整上花费了大量的时间和精力。”论文的第二作者,李朋勇指导的、负责分子片段化算法的2019级本科生章楷豪说,“但正是这种坚持,让我们找到了最优的算法和参数。”
“精准医学的重要基石”
为了验证DeepBlock方法的有效性,团队进行了大量的实验。他们选择了多种不同的靶标蛋白,并使用DeepBlock方法生成了相应的配体分子。结果令人振奋:DeepBlock生成配体的可合成比例得到了大幅度提升,比当前最好方法提升6%,在保持高亲和力的同时具备更高的类药性和分子合理性,平均类药性分数达0.54。此外,在保证与靶标蛋白高亲和力的前提下,DeepBlock还能生成出更低毒性的配体。
“我们用了几种不同的靶标蛋白进行测试,结果都显示DeepBlock方法生成的配体在各个方面都优于传统方法。”李朋勇说,“这让大家对这项技术充满了信心。”
DeepBlock方法的成功引起了广泛关注。国家自然科学基金委员会对该成果进行了报道。此外,希腊雅典国立卡波季斯特里安大学、美国纽约IntelligenciaInc、英国邓迪大学Ninewells医院的专家们也在Nature Computational Science上发表了评论文章,指出 DeepBlock这样的方法可以作为实现精准医学的重要基石。与其他平台结合使用,有望推动分子控制和配体生成的进一步发展,为药物再利用和药物设计的未来提供助力。

国家自然科学基金委报道研究成果
“DeepBlock方法不仅为解决合成难度和毒性控制等实际问题提供了创新的解决方案,也为药物设计提供了全新的思路。”报道中写道,“这将为药物的安全性和有效性提供有力保障。”
开启药物设计新篇章
李朋勇和他的团队并没有止步于此。他们计划进一步优化DeepBlock方法,并将其应用于更多类型的药物设计任务中。此外,他们还希望与更多的制药公司合作,将这项技术转化为实际的产品,造福更多患者。
“我们希望DeepBlock方法能够成为药物设计领域的一个新标准。”李朋勇说,“最终目标是让药物设计变得更加高效、安全和可靠。”
在精准医学的道路上,李朋勇和他的团队将继续前行,迎接新的挑战。目前,团队已经和北大医学部进行合作,进行针对乳腺癌的药物筛选、推荐与验证。未来,团队也将对算法进行下一步优化,推动药物设计从二维结构迈向三维分子生成,提升分子的可合成性和类药性。正如李朋勇所说:“科学研究的魅力就在于,你永远不知道下一步会走向哪里。但正是这种未知,激励着我们不断探索,不断前行。”



